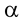ВЫБОР ЗАДАНИЯ И ВАРИАНТА ДЛЯ ВЫПОЛНЕНИЯ КОНТРОЛЬНОЙ РАБОТЫ
1. Номер контрольного задания выбирается в соответствии с предпоследней цифрой номера зачѐтной книжки. Соответствующие ему номера задач для решения указаны в таблице 1.
2. Номер варианта каждой из задач выбирается в соответствии с последней цифрой номера зачѐтной книжки из таблицы к условию соответствующей задачи.
Пример. Номер зачѐтной книжки 02817. По предпоследней цифре зачѐтной книжки выбираем номер задания – задание № 1. По табл. 1 находим, что в задании №1 (предпоследняя цифра зачѐтной книжки) следует решить задачи 1, 2, 5, 7, 9, 11, 14.
Для данных задач выбираем вариант, соответствующий последней цифре зачѐтной книжки (т.е. вариант № 7).
Таблица 1
|
Номер задания
|
Номера задач
|
|
1
|
1, 2, 5, 7, 9, 11, 14.
|
|
2
|
2, 4, 6, 8, 10, 12, 14.
|
|
3
|
1, 3, 5, 8, 11, 13, 14.
|
|
4
|
1, 4, 5, 7, 9, 11, 14.
|
|
5
|
2, 3, 6, 8, 10, 13, 14.
|
|
6
|
1, 4, 6, 7, 9, 11, 14.
|
|
7
|
1, 3, 5, 7, 11, 12, 14.
|
|
8
|
2, 5, 8, 11, 12, 13, 14.
|
|
9
|
1, 3, 5, 8, 10, 12, 14.
|
|
0
|
2, 4, 6, 7, 9, 11, 14.
|
Задача 1. Рассчитать объѐм воздуха и продуктов горения, а также состав продуктов горения (в об. %), образующихся при сгорании m кг вещества (табл. 2), если горение происходит при заданных условиях (табл. 2) и коэффициенте избытка воздуха (табл. 2).
Таблица 2
|
Номер варианта
|
Название вещества
|
Химическая формула
|
Температура
t С
|
Давление P, кПа
|
m
|
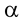
|
|
1
|
Этанол
|
С2Н6О
|
10
|
100,0
|
10
|
1,1
|
|
2
|
Пропанол-1
|
С3Н8О
|
15
|
100,0
|
12
|
1,2
|
|
3
|
Бутанол-1
|
С4Н10О
|
20
|
105,0
|
44
|
1,3
|
|
4
|
Толуол
|
С7Н8
|
25
|
105,0
|
18
|
1,4
|
|
5
|
Анилин
|
С6Н5NН2
|
30
|
105,0
|
97
|
1,5
|
|
6
|
Глицерин
|
С3Н5 (ОН)3
|
35
|
110,0
|
10
|
1,6
|
|
7
|
Этиленгликоль
|
С2Н4 (ОН)2
|
40
|
110,0
|
33
|
1,7
|
|
8
|
Ацетон
|
С3Н6О
|
45
|
110,0
|
26
|
1,8
|
|
9
|
Диэтиловый
эфир
|
С4Н10О
|
50
|
115,0
|
55
|
1,9
|
|
0
|
Пропилацетат
|
С5Н10О2
|
50
|
115,0
|
72
|
1
|
Задача 2. Рассчитать объѐм воздуха и продуктов горения при сгорании горючего газа (табл. 3) объѐмом V м3 при заданных условиях (табл. 3), если горение происходит при избытке воздуха
Таблица 3
|
Номер варианта
|
Название вещества
|
Химическая формула
|
Исходная температура, t С
|
Температура продуктов горения,
t С
|
Объѐм
V, м3
|
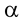
|
|
1
|
Метан
|
СН4
|
30
|
1600
|
1
|
1,4
|
|
2
|
Этан
|
С2Н6
|
25
|
1700
|
2
|
1,3
|
|
3
|
Пропан
|
С3Н8
|
20
|
1800
|
3
|
1,1
|
|
4
|
Бутан
|
С4Н10
|
15
|
1700
|
4
|
1,5
|
|
5
|
Ацетилен
|
С2Н2
|
10
|
2200
|
5
|
1,1
|
|
6
|
Метилэтиловый эфир
|
С3Н8О
|
5
|
1650
|
6
|
1,4
|
|
7
|
Диметиловый эфир
|
С2Н6О
|
35
|
1600
|
7
|
1,6
|
|
8
|
Диметилпропан
|
С5Н12
|
40
|
1700
|
8
|
1,4
|
|
9
|
Сероводород
|
Н2S
|
20
|
1500
|
9
|
1,2
|
|
0
|
Водород
|
Н2
|
10
|
2000
|
10
|
1,3
|
Задача 3. Определить объѐм воздуха, пошедшего на горение, и объем образовавшихся продуктов горения при сгорании смеси газов (табл. 4), если горение происходит при коэффициенте избытка воздуха газовой смеси V, м3.
Объем исходной газовой смеси V, м3.
Таблица 4
|
Состав смеси, %
|
Номер варианта
|
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
0
|
|
Оксид углерода
(II)
|
-
|
10
|
-
|
-
|
-
|
43
|
-
|
10
|
-
|
5
|
|
Водород
|
50
|
-
|
-
|
-
|
-
|
|
-
|
|
25
|
5
|
|
Метан
|
-
|
-
|
20
|
-
|
-
|
36
|
-
|
20
|
|
60
|
|
Этан
|
-
|
-
|
-
|
45
|
45
|
|
24
|
|
5
|
|
|
Пропан
|
-
|
-
|
-
|
-
|
-
|
|
|
14
|
|
|
|
Бутан
|
8
|
-
|
-
|
-
|
20
|
|
|
|
|
|
|
Этилен
|
20
|
22
|
28
|
-
|
|
|
16
|
2
|
|
|
|
Пропен
|
-
|
-
|
-
|
20
|
|
21
|
|
|
|
|
|
Ацетилен
|
-
|
8
|
-
|
|
|
|
10
|
|
20
|
|
|
Углекис-
лый газ
|
20
|
10
|
18
|
20
|
20
|
|
10
|
26
|
|
25
|
|
Азот
|
-
|
50
|
24
|
|
15
|
|
15
|
25
|
30
|
|
|
Кислород
|
2
|
|
10
|
15
|
|
|
25
|
3
|
20
|
5
|
|
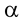
|
1,4
|
1,8
|
1,3
|
1,1
|
1,2
|
1,9
|
1,2
|
1,4
|
1,1
|
1,3
|
|
V, м3
|
100
|
55
|
25
|
10
|
45
|
50
|
75
|
60
|
150
|
35
|
Задача 4. Определить, какое количество вещества (табл. 5) может выгореть в закрытом помещении объѐмом Vп, если известно, что горение прекращается при содержании кислорода в помещении, равном . Для расчѐта коэффициента избытка воздуха рекомендуется воспользоваться формулой (11).
Таблица 5
|
Номер
варианта
|
Название
вещества А
|
Химическая
формула
|
Vп, м3
|
О .
2
|
|
1
|
Ацетон
|
СН3СОСН3
|
100
|
11
|
|
2
|
Бензол
|
С6Н6
|
200
|
12
|
|
3
|
Метанол
|
СН3ОН
|
300
|
13
|
|
4
|
Этанол
|
С2Н5ОН
|
400
|
14
|
|
5
|
Глицерин
|
С3Н5(ОН)3
|
500
|
15
|
|
6
|
Гексан
|
С6Н14
|
600
|
16
|
|
7
|
Диэтиловый
эфир
|
С2Н5ОС2Н5
|
700
|
17
|
|
8
|
Толуол
|
С6Н5СН3
|
800
|
16
|
|
9
|
Стирол
|
С6Н5С2Н3
|
900
|
15
|
|
0
|
Бутонол
|
С4Н9ОН
|
1000
|
14
|
Задача 5. Методом последовательных приближений рассчитать калориметрическую температуру горения для стехиометрической смеси горючего вещества с воздухом (табл. 6). Для расчѐтов использовать данные приложения 10.
Таблица 6
|
Номер
варианта
|
Горючее вещество
|
Химическая формула
|
|
1
|
Толуол
|
С7Н8
|
|
2
|
Анилин
|
С6Н5NН2
|
|
3
|
Глицерин
|
С3Н5(ОН)3
|
|
4
|
Этиленгликоль
|
С2Н4(ОН)2
|
|
5
|
Ацетон
|
С3Н6О
|
|
6
|
Диэтиловый эфир
|
С4Н10О
|
|
7
|
Пропилацетат
|
С5Н10О2
|
|
8
|
Этанол
|
С2Н6О
|
|
9
|
Пропанол-1
|
С3Н8О
|
|
0
|
Бутанол-1
|
С4Н10О
|
Задача 6. Пользуясь средними значениями теплоѐмкостей (табл. 19), рассчитать температуру горения горючего вещества (табл. 7), если горение протекает при коэффициенте избытка воздуха (табл. 7), а доля потерь тепла излучением составляет (табл. 7).
Таблица 7
|
Номер варианта
|
Название вещества
|
Элементный состав вещества, масс. %
|
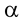
|
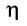
|
|
С
|
Н
|
О
|
S
|
N
|
W
|
зола
|
|
1
|
Антрацит
|
67
|
3
|
4
|
0,5
|
1,0
|
3
|
21,5
|
1,1
|
0,2
|
|
2
|
Горючий
сланец
|
24,2
|
1,8
|
4,5
|
3,0
|
2,0
|
25
|
39,5
|
1,2
|
0,3
|
|
3
|
Керосин
|
80
|
13,7
|
0,3
|
-
|
-
|
6
|
-
|
1,3
|
0,4
|
|
4
|
Бензин
|
85
|
8,0
|
5,0
|
-
|
2,0
|
|
|
1,4
|
0,3
|
|
5
|
Соляровое
масло
|
86,0
|
12,0
|
1,2
|
0,8
|
-
|
-
|
-
|
1,5
|
0,2
|
|
6
|
Мазут
|
84
|
10
|
2
|
3
|
-
|
1
|
-
|
1,6
|
0,3
|
|
7
|
Древесина
|
46
|
6
|
37
|
-
|
2
|
9
|
-
|
1,7
|
0,4
|
|
8
|
Уголь
|
72
|
6
|
4
|
2
|
3
|
13
|
-
|
1,8
|
0,3
|
|
9
|
Церезин
|
85
|
14
|
1
|
-
|
-
|
-
|
-
|
1,7
|
0,2
|
|
0
|
Горючий сланец
|
30
|
5
|
12
|
5
|
2
|
10
|
36
|
1,6
|
0,3
|
Задача 7. Рассчитать, какое количество (в кг) горючей жидкости (табл. 8) должно испариться в закрытом помещении объѐмом Vп при нормальных условиях, чтобы создалась минимальная взрывоопасная концентрация горючих паров. Условно принять, что пары горючей жидкости равномерно распределены в объѐме помещения. Нижний концентрационный предел распространения пламени рассчитать по аппроксимационной формуле.
Таблица 8
|
Номер варианта
|
Название горючей
жидкости
|
Химическая формула
|
Объѐм помещения, м3
|
|
1
|
Этиленгликоль
|
С2Н4(ОН)2
|
200
|
|
2
|
Ацетон
|
СН3СОСН3
|
300
|
|
3
|
Толуол
|
С6Н5СН3
|
400
|
|
4
|
Гексан
|
С6Н14
|
500
|
|
5
|
Глицерин
|
С3Н5(ОН)3
|
600
|
|
6
|
Бензол
|
С6Н6
|
700
|
|
7
|
Пропаноло
|
С3Н7ОН
|
800
|
|
8
|
Этанол
|
С2Н5ОН
|
350
|
|
9
|
Метанол
|
СН3ОН
|
450
|
|
0
|
Бутанол
|
С4Н9ОН
|
550
|
Задача 8. Используя аппроксимационную формулу рассчитать концентрационные пределы распространения пламени и величину предельно допустимой взрывобезопасной концентрации (ПДВК) следующих веществ при заданной температуре t, ºС (табл. 9).
Таблица 9
|
Номер варианта
|
Вещество
|
Температура t, ºС
|
|
1
|
Ацетилен
|
40
|
|
2
|
Водород
|
45
|
|
3
|
Ацетон
|
50
|
|
4
|
Метиловый спирт
|
55
|
|
5
|
Этиловый спирт
|
60
|
|
6
|
Пропиловый спирт
|
65
|
|
7
|
Бутиловый спирт
|
70
|
|
8
|
Бензол
|
75
|
|
9
|
Стирол
|
80
|
|
0
|
Ксилол
|
85
|
Задача 9. Рассчитать концентрационные пределы распространения пламени газовой смеси следующего состава при заданных условиях (табл. 10).
Таблица 10
|
Номер варианта
|
Состав смеси, %
|
Условия среды
|
|
СН4
|
СО
|
Н2
|
Н2О
|
С3Н8
|
t, С
|
Р, кПа
|
|
1
|
25
|
50
|
20
|
5
|
-
|
10
|
90
|
|
2
|
30
|
20
|
30
|
20
|
-
|
15
|
95
|
|
3
|
30
|
20
|
10
|
-
|
40
|
-10
|
90
|
|
4
|
30
|
10
|
20
|
10
|
30
|
65
|
105
|
|
5
|
20
|
25
|
15
|
15
|
25
|
90
|
108
|
|
6
|
40
|
20
|
20
|
-
|
20
|
85
|
110
|
|
7
|
30
|
30
|
10
|
30
|
-
|
60
|
112
|
|
8
|
-
|
45
|
15
|
10
|
30
|
65
|
114
|
|
9
|
40
|
20
|
-
|
10
|
30
|
70
|
112
|
|
0
|
45
|
-
|
25
|
5
|
25
|
75
|
110
|
Задача 10. Рассчитать минимальную флегматизирующую концентрацию инертного разбавителя, об. %, исходя из минимальной адиабатической температуры горения паровоздушной смеси вещества А при разбавлении еѐ флегматизатором Ф (табл. 11), а также минимальное взрывоопасное содержание кислорода и безопасную концентрацию кислорода. Построить график зависимости КПРП от концентрации флегматизатора
Таблица 11
|
Номер
варианта
|
Название вещества
А
|
Химическая
формула
|
Флегматизатор Ф
|
|
1
|
Пентан
|
С5Н12
|
Азот
|
|
2
|
Гексан
|
С6Н14
|
Азот
|
|
3
|
Уксусноэтиловый
эфир
|
СН3СООС2Н5
|
Водяной пар
|
|
4
|
Диэтиловый эфир
|
С4Н10О
|
Водяной пар
|
|
5
|
Этиловый спирт
|
С2Н6О
|
Диоксид углерода
|
|
6
|
Метиловый спирт
|
СН4О
|
Диоксид углерода
|
|
7
|
Ацетон
|
СН3СОСН3
|
Азот
|
|
8
|
Бензол
|
С6Н6
|
Азот
|
|
9
|
Пропилен
|
С3Н6
|
Диоксид углерода
|
|
0
|
Пропиловый спирт
|
С3Н8О
|
Диоксид углерода
|
Задача 11. Рассчитать температурные пределы распространения пламени жидкости (табл. 12) по ее концентрационным пределам распространения пламени, определить взрывобезопасный температурный режим.
Таблица 12
|
Номер варианта
|
Название вещества
|
Химическая формула
|
|
1
|
Метиловый спирт
|
СН3ОН
|
|
2
|
Бутиловый спирт
|
С4Н9ОН
|
|
3
|
Пропиловый спирт
|
С3Н7ОН
|
|
4
|
Аллиловый спирт
|
С3Н5ОН
|
|
5
|
Ацетон
|
С3Н6О
|
|
6
|
Бензол
|
С6Н6
|
|
7
|
Толуол
|
С6Н5СН3
|
|
8
|
Октан
|
С8Н18
|
|
9
|
Стирол
|
С8Н8
|
|
0
|
Этилбензол
|
С8Н10
|
Задача 12. Рассчитать температуру вспышки или температуру воспламенения горючей жидкости (табл. 13) по формуле В.И. Блинова. Определить класс жидкости по пожарной опасности и категорию помещения. Сравнить найденное значение со справочным [3]. При расчѐтах использовать данные приложения 12.
Таблица 13
|
Номер
варианта
|
Название
жидкости
|
Химическая
формула
|
Определяемый параметр
|
|
1
|
Уксусноэтиловый
эфир
|
СН3СООС2Н5
|
Температура вспышки
(о.т.)
|
|
2
|
Толуол
|
С6Н5СН3
|
Температура вспышки
(о.т.)
|
|
3
|
Октан
|
С8Н18
|
Температура
воспламенения
|
|
4
|
Бутилформиат
|
С5Н10О2
|
Температура вспышки
(з.т.)
|
|
5
|
Метиловый спирт
|
СН3ОН
|
Температура вспышки
(о.т.)
|
|
6
|
Этиловый спирт
|
С2Н5ОН
|
Температура вспышки
(о.т.)
|
|
7
|
Бутиловый спирт
|
С4Н9ОН
|
Температура
воспламенения
|
|
8
|
Ацетон
|
С3Н6О
|
Температура
воспламенения
|
|
9
|
Бензол
|
С6Н6
|
Температура вспышки
(з.т.)
|
|
0
|
Пропиловый
спирт
|
С3Н8О
|
Температура вспышки
(з.т.)
|

Задача 13. Используя данные приложений 13, 14, 15 определить стандартную температуру самовоспламенения вещества (табл. 14) по средней длине углеродной цепи, определив число концевых групп и число цепей.
Таблица 14.
|
№ вар-
та
|
Название вещества
|
Структурная формула
|
|
1
|
2,4-диметил-3-этилоктан
|
H3C - CH - CH - CH - CH2 - CH2 - CH2 - CH3 CH3 CH2 CH3
CH3
|
|
2
|
1,2-диметил-4-бутилбензол
|
CH3
H3C - - CH2 - CH2 - CH2 - CH3
|
|
3
|
4-метил-2-этилгексанол-1
|
CH2 - CH3
HO - CH2 - CH - CH2 - CH - CH3
CH2 - CH3
|
|
4
|
1-этил-2-этил-4-пропилбензол
|
CH3
H3C - CH2 - CH2 - CH2 - CH3
|
|
5
|
2,4-диметил-3-этилпентанол-1
|
HO - CH2 - CH - CH - CH - CH3
CH3 CH2 CH3 CH3
|
|
6
|
изопентилбензол
|
CH3 H3C - CH2 - C
CH3
|
|
7
|
3,3,5-триметилгептанол-2
|
CH3
H3C - CH - C - CH2 - CH - CH3 OH CH3 CH2 - CH3
|
|
8
|
3-метил-2-этилгептанол-1
|
CH3
H3C - CH2 - CH2 - CH - CH2 - CH - CH2 - OH
CH2 - CH3
|
|
9
|
2,2,4,4-тетраметилпентан
|
СН3 СН3 СН3 – С – СН2 – С – СН3
СН3 СН3
|
|
0
|
2,2,3-триметилгексан
|
СН3
СН3 – С – СН – СН2 – СН2 - СН3 СН3 СН3
|
Задача 14. Сферический заряд ТНТ (тринитротолуол) массой W (табл. 15) взрывается при стандартных атмосферных условиях. Найти параметры падающей (рис. 5) и нормально отражѐнной от препятствия (рис. 6) взрывной волны на расстоянии R (табл. 15) от центра взрыва.
Таблица 15.
|
Номер варианта
|
Масса ТНТ W, кг
|
Расстояние R, м
|
|
1
|
5
|
150
|
|
2
|
10
|
100
|
|
3
|
15
|
50
|
|
4
|
6
|
30
|
|
5
|
8
|
10
|
|
6
|
10
|
80
|
|
7
|
2
|
250
|
|
8
|
4
|
300
|
|
9
|
6
|
350
|
|
0
|
20
|
400
|
|